Os Átomos e Sua Estrutura
Primeiramente, para uma compreensão básica dos conceitos de tensão e corrente, é necessário ter uma familiaridade com o átomo e sua estrutura.
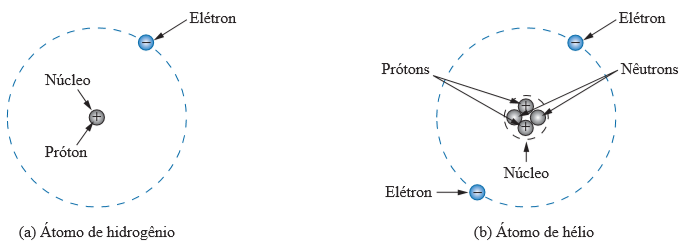
O átomo mais simples é o hidrogênio, constituído por duas partículas: o próton e o elétron. O proton é o núcleo do hidrogênio e possui uma carga positiva. Por outro lado, o elétron tem carga negativa e orbita ao redor do núcleo. As partículas positivas e negativas possuem a mesma carga em módulo.
No caso de outros elementos, o núcleo também contém neutrons, que têm massa ligeiramente maior que a do próton e não possuem carga elétrica.

Átomos com a última camada completa são considerados estáveis. Enquanto átomos com uma pequena porcentagem da última camada completa são normalmente instáveis e voláteis, pois esse(s) elétrons tem menos força de atração com o núcleo.
A força de atração entre o elétron e o núcleo pode ser calculada pela lei de Coulomb.

Para uma explicação mais detalhada e extensa sobre os átomos, sua estrutura e comportamento, visite nossa página de Eletrostática.